Ficin fehérjehidrolízishez: adagolás, pH és hőmérséklet hibaelhárítása
Oldja meg a ficin fehérjehidrolízishez kapcsolódó problémáit gyakorlati adagolási, pH-, hőmérsékleti, QC-, pilot-validálási és beszállító-minősítési útmutatóval.

Azoknál a gyártóknál, akik a ficin enzimet fehérjehidrolízishez értékelik, a folyamat teljesítménye az enzimaktivitás, a szubsztrát, a pH, a hőmérséklet, a tartózkodási idő és a downstream kontrollok összehangolásától függ.
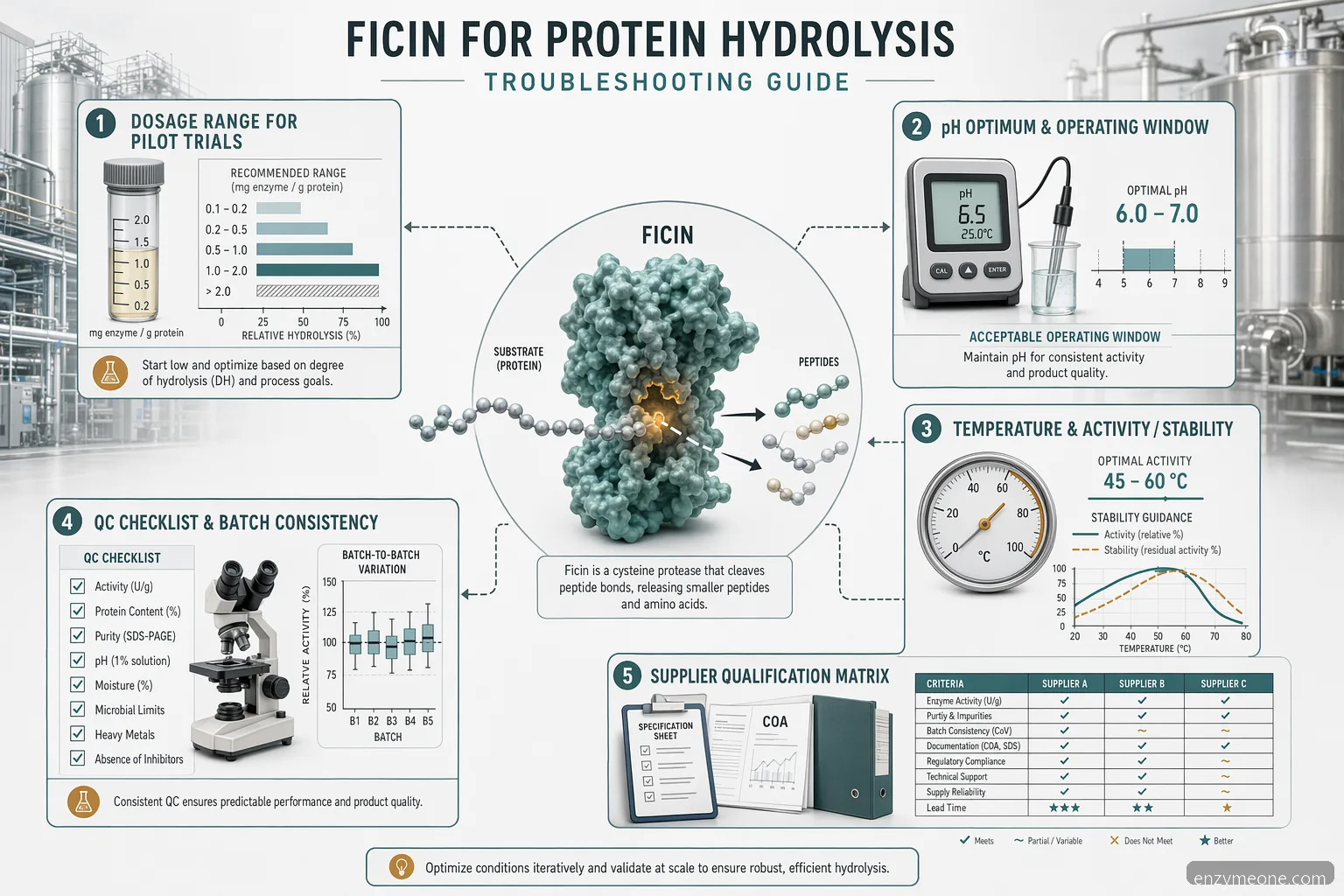
Miért viselkedik a ficin eltérően a fehérjehidrolízisben
A ficin növényi eredetű proteáz, amelyet gyakran a füge latexével társítanak, ezért a vevők a fehérjehidrolízishez használt fügeenzimre is kereshetnek. Ipari rendszerekben fehérjeszubsztrátok kisebb peptidekre bontására, oldhatóság javítására, textúra módosítására vagy funkcionális összetevők előállításának támogatására használják. A teljesítmény a szubsztráttól, az előkezeléstől, a sótartalomtól, a szárazanyag-tartalomtól és a beszállító aktivitásvizsgálatától függően változhat. Ami kollagénen, húsnyesedéken, növényi fehérjén vagy zselatinon működik, az nem feltétlenül vihető át közvetlenül tejipari, tengeri vagy vegyes fehérjeáramokra. Hibaelhárításkor tisztázza, hogy a cél a gyors viszkozitáscsökkentés, a szabályozott peptidmret, a jobb emészthetőség, az ízképzés vagy a kihozatal javítása. Minden cél eltérő végpontot és enzim-inaktiválási lépést igényelhet. Az ipari ficin enzimes fehérjehidrolízist ezért laboratóriumi szűréssel, majd pilot-validálással kell fejleszteni, ugyanazon keverési, fűtési és tartási feltételek mellett, amelyek a gyári méretben várhatók.
Határozza meg a kívánt hidrolízis-végpontot az adagolás kiválasztása előtt. • Hasonlítsa össze a beszállítókat az enzimaktivitás és az alkalmazási teljesítmény alapján. • Valós szubsztráton validáljon, ne csak modellfehérjéken.
Kiinduló adagolási tartományok pilot vizsgálatokhoz
A ficin fehérjehidrolízishez történő alkalmazásánál az adagolást lehetőleg aktivitási egység/kilogramm fehérje vagy szubsztrát formájában kell megadni, amennyiben a fehérjehidrolízishez használt ficin enzim beszállítója validált aktivitásmódszert biztosít. Ha csak százalékos hozzáadás áll rendelkezésre, használja szűrési referenciaként, és a COA kézhezvétele után alakítsa át. Gyakorlati pilot tartományként gyakran 0.02% és 0.50% közötti enzimtermék/szubsztrát tömeg arány használható, az aktivitáskoncentrációtól, a fehérje hozzáférhetőségétől, a szárazanyag-tartalomtól, az időtől és a szükséges hidrolízisfoktól függően. Alacsony adagok alkalmasak lehetnek textúramódosításra vagy enyhe oldásra, míg magasabb adagok szükségesek lehetnek keményebb kötőszövet vagy nagy szárazanyag-tartalmú zagyok esetén. Ne feltételezze, hogy a több enzim mindig alacsonyabb fajlagos költséget jelent. A túlzott hidrolízis keserűséget növelhet, csökkentheti a funkcionális szerkezetet, szűrési problémákat okozhat, vagy további downstream korrekciót tehet szükségessé. Készítsen adagolási görbét legalább három enzim-szinttel és egy enzim nélküli kontrollal.
Szűrje alacsony, közepes és magas adagokkal azonos körülmények között. • Lehetőség szerint normalizálja az eredményeket aktivitási egységekre. • A kész hidrolizátum kilogrammonkénti költségét értékelje, ne csak a beszerzési árat.
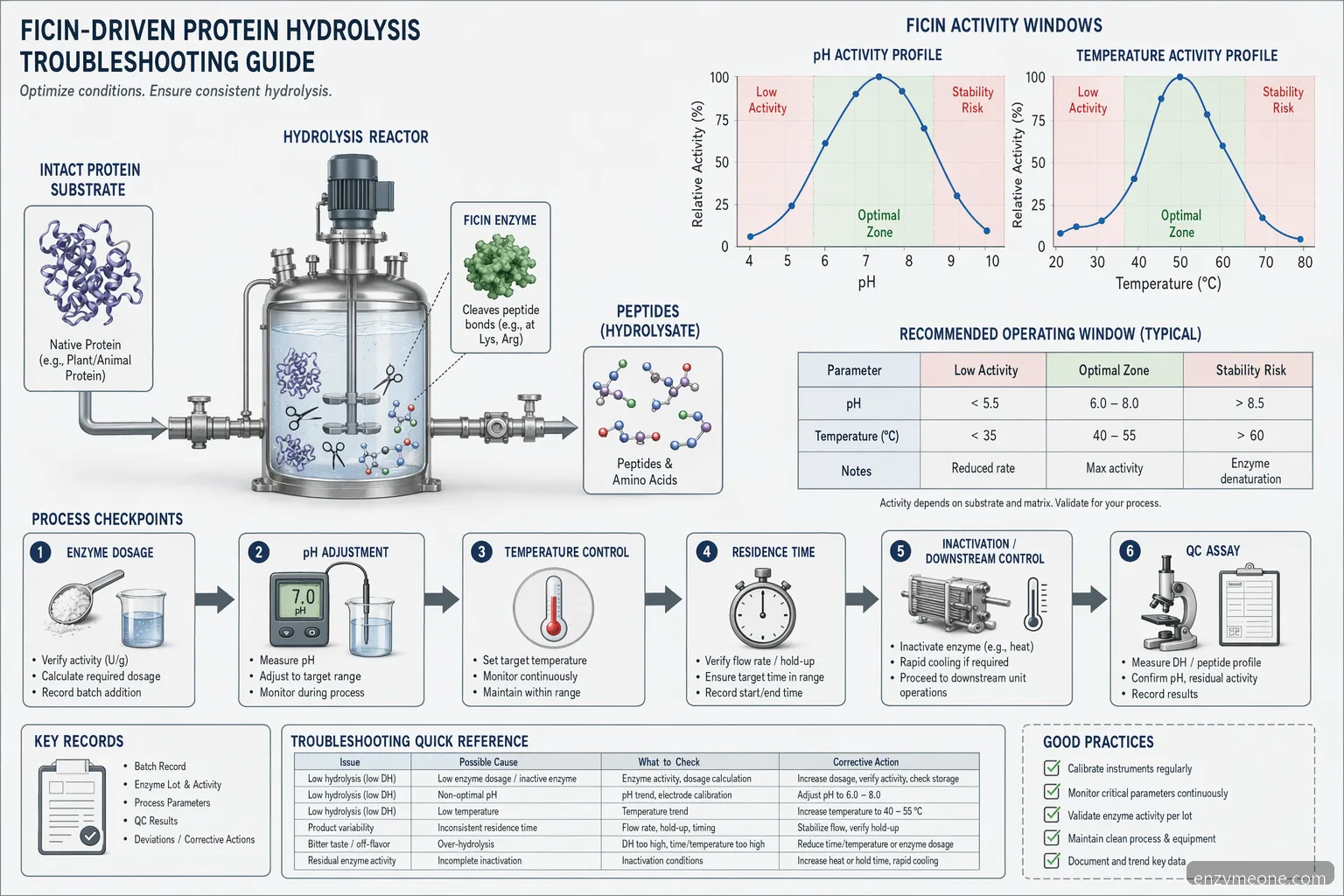
pH- és hőmérséklet-hibaelhárítás
A ficin jellemzően enyhén savas és közel semleges folyamatablakban teljesít a legjobban, de az ideális pH-t a beszállító TDS-e és a tényleges szubsztrát alapján kell megerősíteni. Gyakori szűrési tartomány a pH 5.0 és 7.5 között, majd a finomhangolás az oldható nitrogén és a peptideloszlás mérése után történik. A hőmérsékleti szűrés gyakran 40°C és 60°C körül indul. Az alacsonyabb hőmérséklet megóvhatja az érzékeny ízjegyeket, vagy csökkentheti a mikrobiológiai kockázatot rövid tartási idővel kombinálva, míg a magasabb hőmérséklet javíthatja a reakciósebességet, amíg az enzim stabilitása nem romlik. Ha a hidrolízis lelassul, ellenőrizze a pH-eltolódást a szubsztrát pufferhatása, a savadagolás, az ásványi sók vagy a felszabaduló aminos csoportok miatt. Ha a teljesítmény a felskálázás után romlik, ellenőrizze a felfűtési időt, a tartályon belüli hőmérsékleti gradienseket, a nyírást és a tényleges termékhőmérsékletet, ne csak a köpenyhőmérsékletet. Szabályozott gyártás esetén határozza meg mind az aktív hidrolízis hőmérsékletét, mind a reakció leállítására használt termikus inaktiválási feltételt.
Kezdeti pH-szűrés: jellemzően pH 5.0 és 7.5 között. • Kezdeti hőmérsékleti szűrés: jellemzően 40°C és 60°C között. • A végső beállításokat a beszállító TDS-e és a gyári próbák alapján erősítse meg. • Dokumentálja az enzim inaktiválását a további hidrolízis megelőzésére.
QC ellenőrzések, amelyek megelőzik a tételenkénti eltéréseket
Az ipari ficin fehérjehidrolízis az egyszerű megjelenés- és kihozatalvizsgálaton túl analitikai kontrollt igényel. Kövesse a pH-t a hozzáadás előtt, a tartási idő alatt és a végpontnál. Mérje a hőmérsékletet a tartály reprezentatív pontjain. A terméktől függően a QC magában foglalhatja a hidrolízisfokot, az oldható nitrogént, a szabad aminos nitrogént, a peptid molekulatömeg-eloszlást, a viszkozitást, a zavarosságot, a szűrési sebességet, a nedvességet, a hamut, a mikrobiológiai indikátorokat és az olyan érzékszervi jegyeket, mint a keserűség vagy a kénes jegyek. Hibaelhárításkor őrizzen meg mintákat minden időpontból, és hasonlítsa össze őket egy korábban elfogadott tétellel. Ha egy tétel alulhidrolizált, vizsgálja felül az enzim tárolását, a tétel aktivitását, az adagolási pontosságot, a keverést, a tartózkodási időt és a szubsztrát előkezelését. Ha egy tétel túlhidrolizált, csökkentse a tartási időt, az adagolást vagy a hőmérsékletet, és erősítse meg a leállítási lépést. A gyakorlati specifikációnak tartalmaznia kell mind a folyamatparamétereket, mind a késztermék funkcionális eredményeit, mivel ugyanaz a hidrolízisfok különböző szubsztrátokon eltérően viselkedhet.
Felskálázás során alkalmazzon időpont-alapú mintavételezést. • Tartson meg mintákat az elfogadott és a selejtezett tételekből. • Kapcsolja össze a QC eredményeket a funkcionális teljesítménnyel, ne csak a kémiai értékekkel.
Hogyan minősítsen egy ficin beszállítót
A fehérjehidrolízishez minősített ficin beszállítónak minden tételhez aktuális COA-t, az aktivitás meghatározását és az ajánlott felhasználási feltételeket tartalmazó TDS-t, valamint biztonságos kezeléshez SDS-t kell biztosítania. A vevőknek meg kell kérdezniük, hogyan mérik az aktivitást, a termék por vagy folyadék-e, mik az ajánlott tárolási feltételek, mi a hordozó összetétele, milyen allergén- és szabályozási információk relevánsak az adott piacra, valamint mennyi a várható eltarthatóság. Mivel az aktivitásvizsgálatok eltérhetnek, a beszállítókat a saját szubsztrátrendszerében hasonlítsa össze, ne csak a címkén szereplő erősség alapján. Kérjen pilot mennyiségeket a fehérjehidrolízishez használt fügeenzim beszállítójától, és végezzen egymás melletti próbákat a jelenlegi folyamatcélhoz képest. A beszállítóértékelésnek tartalmaznia kell a tételenkénti konzisztenciát, a dokumentációs reagálóképességet, a szállítási időt, a csomagolás alkalmasságát, a műszaki támogatást és a fajlagos költséget. A legjobb választás nem mindig a legalacsonyabb egységár; az az enzim a megfelelő, amely megbízhatóan, kereskedelmi méretben teljesíti a szükséges hidrolízis-végpontot.
Kérjen COA-t, TDS-t, SDS-t és tételkövethetőséget. • Erősítse meg az aktivitásmódszert és a tárolási követelményeket. • Végezzen egymás melletti pilot próbákat a kereskedelmi jóváhagyás előtt. • Számítsa ki a fajlagos költséget a tényleges végponti teljesítmény alapján.
Műszaki beszerzési ellenőrzőlista
Vevői kérdések
Gyakorlati szűrési tartományként gyakran 0.02% és 0.50% közötti enzimtermék/szubsztrát tömeg arány használható, de a jobb alap az aktivitási egység/kilogramm fehérje vagy szubsztrát. Készítsen adagolási görbét legalább három szinttel és egy enzim nélküli kontrollal. Válassza azt az adagolást, amely a szükséges végpontot a legalacsonyabb megbízható fajlagos költséggel éri el, túlzott hidrolízis nélkül.
Sok ficin folyamatot pH 5.0 és 7.5 között szűrnek, majd a szubsztrát és a beszállító TDS-e alapján szűkítenek. A legjobb pH az, amely a valós gyári körülmények között a kívánt peptidprofilt, oldhatóságot, ízt és kihozatalt biztosítja. Figyelje a pH-eltolódást a reakció során, mert a fehérjepufferelés és a felszabaduló aminos csoportok megváltoztathatják a tényleges üzemi pontot.
Gyakori pilot szűrési tartomány a 40°C és 60°C közötti érték. A magasabb hőmérséklet növelheti a hidrolízis sebességét, de csak addig, amíg az enzimstabilitás vagy a termékminőség nem válik korlátozó tényezővé. Ellenőrizze a tartály tényleges termékhőmérsékletét, ne csak a köpenybeállításokat. Amint elérte a végpontot, alkalmazzon validált inaktiválási lépést a további proteolízis leállítására és a tételkonzisztencia védelmére.
A beszállítókat a saját szubsztrátjában mutatott teljesítmény alapján hasonlítsa össze, ne csak az ár vagy a címkén szereplő aktivitás alapján. Kérjen COA-t, TDS-t, SDS-t, aktivitásmódszert, tárolási feltételeket, eltarthatóságot és nyomonkövethetőséget. Lehetőség szerint végezzen egymás melletti pilot próbákat azonos aktivitásadagokkal. Ezután számítsa ki a fajlagos költséget a végpont eléréséhez szükséges idő, a kihozatal, a szűrési viselkedés, a minőségi eredmények és a kereskedelmi méretű megbízhatóság alapján.
A keserűség vagy a túlzott viszkozitásvesztés gyakran túlhidrolízisre, magas adagolásra, hosszú tartózkodási időre, emelt hőmérsékletre vagy késedelmes inaktiválásra utal. Tekintse át az időpont-mintákat, a végponti adatokat és az adagolási nyilvántartásokat. Egy korrekciós próba csökkentheti az enzim szintjét, rövidítheti a tartási időt, mérsékelheti a hőmérsékletet, vagy szigoríthatja a leállítási lépést. Az érzékszervi és peptidprofil-vizsgálatok segíthetnek meghatározni az elfogadható üzemi ablakot.
Kapcsolódó keresési témák
ipari ficin fehérjehidrolízis, ipari ficin enzim fehérjehidrolízis, ficin beszállító fehérjehidrolízishez, ficin enzim beszállító fehérjehidrolízishez, ficin enzim fehérjehidrolízishez, ipari fügeenzim fehérjehidrolízis
Ficin for Research & Industry
Need Ficin for your lab or production process?
ISO 9001 certified · Food-grade & research-grade · Ships to 80+ countries
Gyakran ismételt kérdések
Milyen adagolást használjunk a ficin enzim fehérjehidrolízishez?
Gyakorlati szűrési tartományként gyakran 0.02% és 0.50% közötti enzimtermék/szubsztrát tömeg arány használható, de a jobb alap az aktivitási egység/kilogramm fehérje vagy szubsztrát. Készítsen adagolási görbét legalább három szinttel és egy enzim nélküli kontrollal. Válassza azt az adagolást, amely a szükséges végpontot a legalacsonyabb megbízható fajlagos költséggel éri el, túlzott hidrolízis nélkül.
Melyik pH a legjobb az ipari ficin enzim fehérjehidrolízishez?
Sok ficin folyamatot pH 5.0 és 7.5 között szűrnek, majd a szubsztrát és a beszállító TDS-e alapján szűkítenek. A legjobb pH az, amely a valós gyári körülmények között a kívánt peptidprofilt, oldhatóságot, ízt és kihozatalt biztosítja. Figyelje a pH-eltolódást a reakció során, mert a fehérjepufferelés és a felszabaduló aminos csoportok megváltoztathatják a tényleges üzemi pontot.
Milyen hőmérsékletet használjunk a ficinnel végzett fehérjehidrolízishez?
Gyakori pilot szűrési tartomány a 40°C és 60°C közötti érték. A magasabb hőmérséklet növelheti a hidrolízis sebességét, de csak addig, amíg az enzimstabilitás vagy a termékminőség nem válik korlátozó tényezővé. Ellenőrizze a tartály tényleges termékhőmérsékletét, ne csak a köpenybeállításokat. Amint elérte a végpontot, alkalmazzon validált inaktiválási lépést a további proteolízis leállítására és a tételkonzisztencia védelmére.
Hogyan hasonlítsuk össze a ficin beszállítót fehérjehidrolízishez?
A beszállítókat a saját szubsztrátjában mutatott teljesítmény alapján hasonlítsa össze, ne csak az ár vagy a címkén szereplő aktivitás alapján. Kérjen COA-t, TDS-t, SDS-t, aktivitásmódszert, tárolási feltételeket, eltarthatóságot és nyomonkövethetőséget. Lehetőség szerint végezzen egymás melletti pilot próbákat azonos aktivitásadagokkal. Ezután számítsa ki a fajlagos költséget a végpont eléréséhez szükséges idő, a kihozatal, a szűrési viselkedés, a minőségi eredmények és a kereskedelmi méretű megbízhatóság alapján.
Miért lett keserű vagy túl híg a ficines hidrolízis tételünk?
A keserűség vagy a túlzott viszkozitásvesztés gyakran túlhidrolízisre, magas adagolásra, hosszú tartózkodási időre, emelt hőmérsékletre vagy késedelmes inaktiválásra utal. Tekintse át az időpont-mintákat, a végponti adatokat és az adagolási nyilvántartásokat. Egy korrekciós próba csökkentheti az enzim szintjét, rövidítheti a tartási időt, mérsékelheti a hőmérsékletet, vagy szigoríthatja a leállítási lépést. Az érzékszervi és peptidprofil-vizsgálatok segíthetnek meghatározni az elfogadható üzemi ablakot.
Kapcsolódó: Ficin enzim felhasználása ipari proteolízishez
Alakítsa ezt az útmutatót beszállítói briefgé. Kérjen ficin COA-t, TDS-t, SDS-t és pilot mintát a fehérjehidrolízis validálásához. Tekintse meg alkalmazási oldalunkat a Ficin enzim felhasználása ipari proteolízishez témában a /applications/ficin-enzyme-uses/ címen, ahol specifikációk, MOQ és ingyenes 50 g minta található.
Contact Us to Contribute